Данный сайт содержит
профессиональную специализированную информацию
Согласно действующему законодательству, данные материалы могут быть доступны только медицинским работникам. Я подтверждаю, что являюсь специалистом с медицинским образованием, и информация, полученная на сайте, будет использована мною только в профессиональной деятельности.



Дальнейшее использование Вами сайта означает принятие Условий его использования, либо Вам следует покинуть сайт. Сайт может использовать файлы cookie и аналогичные технологии для взаимодействия с Вами. Вы можете согласиться на использование cookie, нажав кнопку «Соглашаюсь» или заблокировать их использование, изменив настройки вашего интернет-браузера.
Дальнейшее использование Вами сайта означает принятие Условий его использования, либо Вам следует покинуть сайт. Сайт может использовать файлы cookie и аналогичные технологии для взаимодействия с Вами. Вы можете согласиться на использование cookie, нажав кнопку «Соглашаюсь» или заблокировать их использование, изменив настройки вашего интернет-браузера.
Тедуглутид у пациентов детского возраста


ООО «Такеда Фармасьютикалс»
119048, г. Москва, ул. Усачева, дом 2, стр. 1
Тел.: 8 800 700 55 11, факс: +7 (495) 502-16-25
www.takeda.com/ru-ru
Тел.: 8 800 700 55 11, факс: +7 (495) 502-16-25
www.takeda.com/ru-ru

Ваши вопросы —
наши ответы!
Сервис научно-медицинской информации для специалистов здравоохранения

VV-MEDMAT-109730
© 2024 Takeda, все права защищены.
Размещенная информация не является рекомендацией компании Такеда, рекламой компании или ее продукции, не должна быть основанием для принятия каких-либо решений или осуществления каких-либо действий. Решение о выборе метода лечения конкретного пациента должно приниматься лечащим врачом.



ТЕДУГЛУТИД —
это первый и единственный препарат, одобренный для пациентов с синдромом короткой кишки с кишечной недостаточностью (СКК-КН)1,2
это первый и единственный препарат, одобренный для пациентов с синдромом короткой кишки с кишечной недостаточностью (СКК-КН)1,2




- Адаптировано из Проекта Клинических рекомендаций по диагностике и лечению синдрома короткой кишки с кишечной недостаточностью у взрослых. Российская гастроэнтерологическая ассоциация https://www.gastro.ru/userfiles
- Адаптировано из Шеменкова ВС. Принципы ведения больных с синдромом короткой кишки. Медицинский Совет. 2023;(23):144-148. https://doi.org
- Pironi L, Arends J, Bozzetti F, et al. Clin Nutr. 2016;35(2):247-307.
- Carter BA, et al. J Pediatr 2017;181:102–11.
- Kocoshis SA, et al. J Parenter Enteral Nutr 2019; doi: 10.1002/jpen.1690 (ePub ahead of print).
- Hofstetter S, Stern L, Willet J, et al. Curr Med Res Opin. 2013;29(5):495-504.
- Jeppesen PB, Sanguinetti EL, Buchman A, et al. Gut. 2005;54(9):1224-1231.
Источники
12-недельное исследование:
TED-C13-0034
TED-C13-0034
- Открытое многоцентровое клиническое исследование
- у 42 пациентов детского возраста от 1 до 17 лет с СКК продолжительностью ≥12 месяцев до скрининга, требующего ПП/ИТ (≥30% калорийности и/или потребности в жидкости/ электролитах)
- Три дозировки Тедуглутида: 0,0125 мг/кг/сут (n=8), 0,025 мг/кг/сут (n=14) и 0,05 мг/кг/сут (n=15); 5 – когорту стандартной терапии
24-недельное исследование:
TED-C14-0065
TED-C14-0065
- Рандомизированное двойное слепое многоцентровое исследование, проведенное
- у 59 пациентов детского возраста от 1 года до 17 лет с СКК, развившимся в результате обширной резекции кишечника, требовавшим поддержки ПП/ВВ (≥30% калорийности и/или потребности жидкости/ электролитах) в течение ≥3 мес. до скрининга
- Две дозировки тедуглутида: 0,025 мг/кг/сут (n=24) и 0,05 мг/кг/сут (n=26); 9 пациентов были включены в когорту стандартной терапии
Большинство НЯ были легкой или средней степени тяжести
Связанными с лечением НЯ, которые имели место: у 2 (4%) пациентов, получавших Тедуглутид, были кровоизлияния в месте инъекции, боли в животе и рвота
Количество пациентов с нежелательными явлениями (НЯ) было одинаковым во всех группах лечения
Связанные с лечением НЯ наблюдались у 8 (33%) пациентов в группе 0,025 мг/кг/сут и у 7 (27%) пациентов в группе 0,05 мг/кг/сут
Тедуглутид у пациентов детского возраста
Объем ЭП
Время инфузии
Объем ПП
Калорийность
Полный отказ от парентерального питания (ПП)
- Три пациента (3/15, 20%), получавшие Тедуглутид в дозе 0,05 мг/кг/сут, прекратили ПП к 12 неделе и 1 в группе 0,025 мг/кг/сут.
- После 4-недельного периода вымывания у двух из этих пациентов ПП было возобновлено, а еще двое остались независимы от ПП.
Снижение объема ПП
- К 16-й неделе снижение ПП все еще наблюдалось, но было выражено в меньшей степени, чем на 12-й неделе.
Безопасность
- Тедуглутид в дозе 0,05 мг/кг/сут характеризуется профилем безопасности, сопоставимым с таковым у взрослых пациентов.
Тедуглутид4-7:
Тедуглутид имитирует естественный ГПП-2 (и улучшает абсорбцию у пациентов с СКК).
Тедуглутид изучали в 2 регистрационных клинических исследованиях; 12-недельное открытое клиническое исследование у 42 детей и 24-недельное рандомизированное двойное слепое многоцентровое исследование у 59 пациентов.
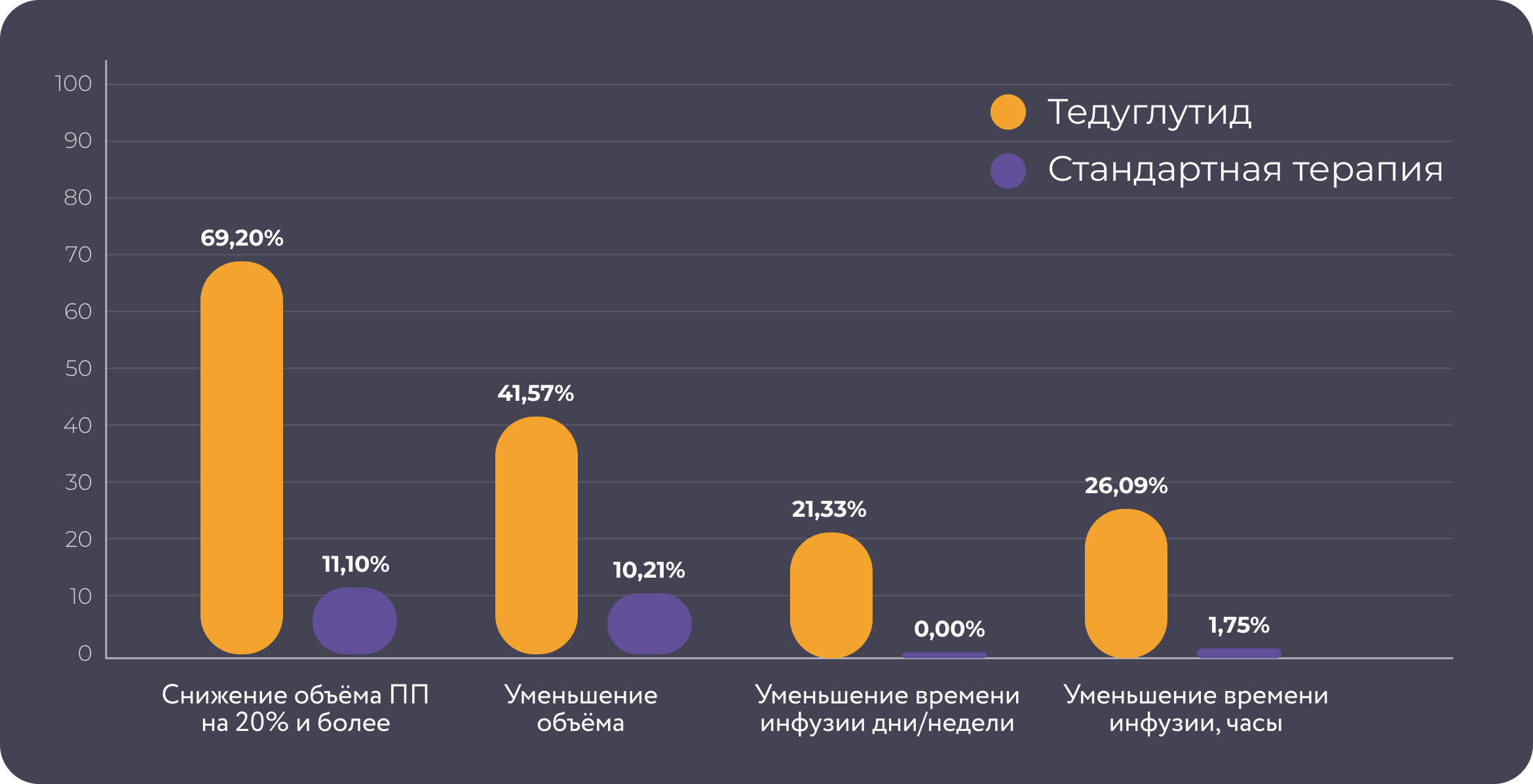
В 24-недельном клиническом исследовании:
- 69% пациентов достигли 20% снижение объема ПП/ИТ от исходного уровня в сравнении с 11% пациентов в группе стандартной терапии.
- Большее снижение объема ПП/ИТ было достигнуто в группе Тедуглутида в сравнении с группой стандартной терапии.
- Тедуглутид обеспечил клинически значимое снижение числа дней ПП/ИТ в неделю к 24 неделе.
- Больше пациентов достигли энтеральной автономии при приеме препарата Тедуглутид в сравнении со стандартной терапией через 24 недели лечения.
Большинство НЯ были легкой или средней степени тяжести.